Células madre mesenquimales: definición, origen histórico y relevancia biomédica
Definición
Las células madre o troncales mesenquimales (CTM) constituyen una población específica de células indiferenciadas caracterizadas por un alto potencial proliferativo. Estas células presentan dos propiedades fundamentales: la capacidad de autorrenovación, que les permite generar células idénticas a la original, y la capacidad de diferenciación hacia uno o varios linajes celulares especializados.
En general, las CTM son consideradas multipotenciales, ya que pueden dar origen a diversos tipos celulares derivados de tejidos adultos, como osteoblastos, condrocitos y adipocitos (Mayani H., Arch Med Res, 2003). Estas propiedades han despertado un creciente interés científico, particularmente por su relevancia en procesos de reparación y regeneración tisular.
En las últimas décadas, el interés por las CTM ha aumentado de manera significativa debido, además, a la posibilidad de aislarlas a partir de tejidos comúnmente desechados, como la placenta, el cordón umbilical o el tejido endometrial, lo que amplía su potencial aplicación en investigación biomédica y medicina regenerativa.
Descubrimiento y primeros estudios
La investigación sobre las células troncales mesenquimales se inició a finales de la década de 1960 y principios de los años 70, cuando Friedenstein y colaboradores describieron, por primera vez, una población de células adherentes derivadas de la médula ósea con capacidad para formar colonias fibroblastoides (CFU-F) y contribuir al estroma hematopoyético (Friedenstein AJ et al., Transplantation, 1968; Exp Hematol, 1978).
Estos estudios pioneros demostraron que dichas células no solo formaban parte del microambiente hematopoyético, sino que además poseían propiedades distintivas como la autorrenovación, una elevada capacidad proliferativa y el mantenimiento de un estado indiferenciado bajo condiciones adecuadas de cultivo.
Posteriormente, durante la década de 1980, diversos grupos de investigación profundizaron en la caracterización funcional de estas células, demostrando su capacidad para diferenciarse en tejidos mesodérmicos como hueso, cartílago y estroma medular. Experimentos en modelos animales confirmaron su notable plasticidad celular (Owen M., Friedenstein AJ., 1988).
Avances en la investigación de las Células Troncales Mesenquimales.
En 1983, Piersma y colaboradores demostraron que la médula ósea contenía progenitores fibroblastoides capaces de ser trasplantados junto con células hematopoyéticas, lo que evidenció su participación activa en la regeneración tisular (Haematologica, 1983). Estudios posteriores realizados por Owen y otros investigadores confirmaron que estas células podían originar tejido óseo, cartilaginoso y conjuntivo, incluso a partir de pequeñas cantidades de médula ósea, resaltando su elevado potencial proliferativo y diferenciativo (Bab I., J Cell Sci, 1986).
Durante este periodo se consolidó el término “células madre mesenquimales”, en referencia a su origen en tejidos adultos y a su capacidad de generar distintos tipos celulares del linaje mesenquimal. Más adelante, se comprobó que estas células no se encontraban exclusivamente en la médula ósea, sino también en otros tejidos adultos como el hígado, pulmón, tracto gastrointestinal, piel y músculo esquelético (Ashton BA., Clin Orthop Relat Res, 1980).
Diversidad de fuentes de células troncales mesenquimales y su aislamiento
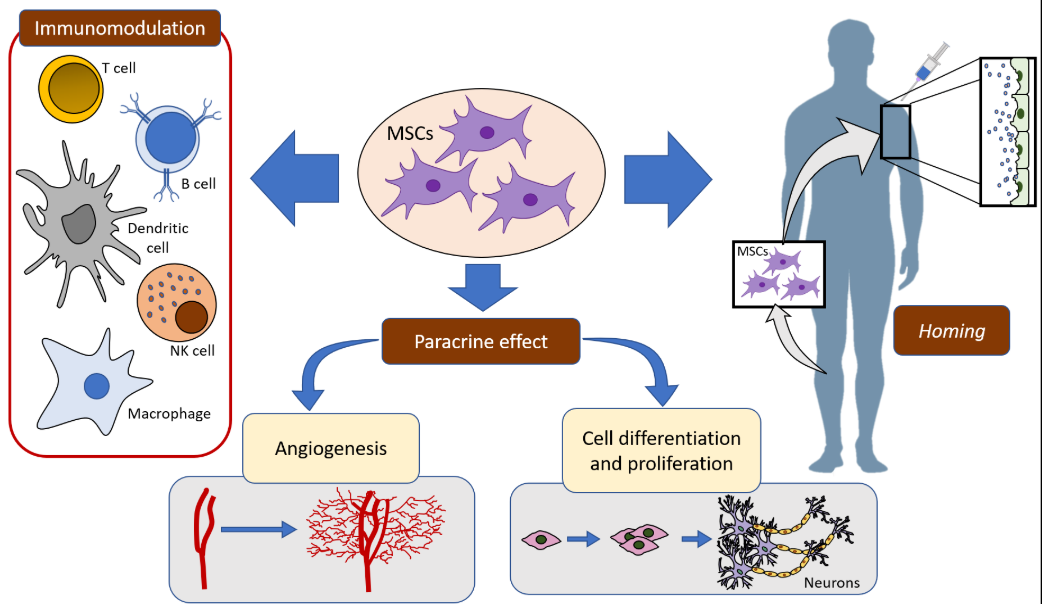
Con el avance de la investigación, se identificaron orígenes celulares alternativos de CTM que ofrecen ventajas relevantes, como su fácil acceso y la reducción de procedimientos invasivos, lo que ha favorecido su aplicación en investigación básica y medicina regenerativa (Gargett & Masuda, 2010).
Aunque el aislamiento de CTM a partir de médula ósea, líquido amniótico o tejido adiposo puede resultar técnicamente complejo y requerir procedimientos quirúrgicos, se han descrito fuentes más accesibles, entre ellas el endometrio humano.
Estudios recientes han demostrado que las células localizadas en la capa basal del endometrio presentan características propias de células madre, incluyendo una alta capacidad proliferativa, autorrenovación y potencial de diferenciación (Mesenchymal stem cells for restoring endometrial function: An infertility perspective).
Si bien el acceso directo al endometrio mediante biopsia o curetaje puede ocasionar daño tisular, se ha identificado una alternativa no invasiva: el aislamiento de células madre mesenquimales derivadas del tejido endometrial. Estas células cumplen con los criterios establecidos por la Sociedad Internacional de Terapia Celular (ISCT), mostrando fenotipo, capacidad de diferenciación y comportamiento funcional característicos de las CTM.
Desde las primeras evidencias publicadas hace más de una década, se ha confirmado la presencia de poblaciones de células madre adultas en el endometrio con capacidad de formar colonias clonales y participar activamente en la reparación y regeneración del tejido endometrial (Taylor, 2004). Revisiones posteriores, como las publicadas en Human Reproduction Update, reforzaron estos hallazgos al demostrar que el endometrio humano contiene células madre/progenitoras con potencial de autorrenovación, diferenciación y reconstrucción tisular (Rungsiwiwut et al., 2020).
Conclusiones y perspectivas
Las células troncales mesenquimales representan uno de los avances más relevantes en el campo de la biología celular y la medicina regenerativa. Desde su identificación inicial en la médula ósea en la década de 1970, se ha demostrado su capacidad para diferenciarse en múltiples linajes celulares y su presencia en diversos tejidos adultos.
El descubrimiento de fuentes alternativas, como el endometrio y la sangre menstrual, ha ampliado de manera significativa el panorama terapéutico de las CTM, al ofrecer métodos de obtención más accesibles, con menor riesgo y consideraciones éticas reducidas.
En conjunto, los avances en el estudio de las CTM han permitido comprender mejor los mecanismos implicados en la regeneración tisular y han sentado las bases para el desarrollo de terapias celulares cada vez más seguras, eficaces y estandarizadas.